Biochimica | Serin-Proteasi, Meccanismo Catalitico,
Автор: BiochimicaSenzaPretese
Загружено: 2022-05-21
Просмотров: 7366
Le serin-proteasi sono la classe di proteasi più rappresentata. Ne abbiamo diversi esempi: la trombina ( enzima convertente fibrinogeno in fibrina), l'elastasi neutrofilica ( degrada i polimeri di elastina), chimotripsina etc.
Vengono dette cosi perchè nel sito attivo ritroviamo un residuo di serina chiave per la reazione ( si comporterà da nucleofilo verso il carbonio carbonilico), questa serina si ritrova insieme ad altri due residui, istidina e aspartato andando a comporre la triade catalitica.
Sono idrolasi, cioè nel loro meccanismo catalitico utilizzano una molecola di acqua per poter rompere l'intermedio acil-enzima che si crea tra una parte del substrato e il residuo di serina.
Una volta attivate vengono inibite, dopo poco tempo, in diversi modi, quello più specifico sono le serpina ( inibitori covalenti di serin-proteasi).
Legenda:
0:00 introduzione sulle serin-proteasi
2:30 Esempio della trombina come serin-proteasi
6:27 Caratteristiche del legame peptidico (ammidico)
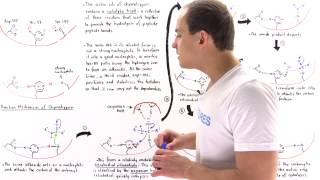
7:33 Meccanismo catalitico

Доступные форматы для скачивания:
Скачать видео mp4
-
Информация по загрузке: