Вывод основных термодинамических уравнений (химия/физика)
Автор: Casual Chemistry
Загружено: 2021-04-27
Просмотров: 6507
Объединяя первый и второй законы термодинамики, а затем вводя энтальпию и энергию Гиббса. Это либо химия, либо физика, либо просто наука.
#химия #физика #термодинамика #стержень #энтальпия #энтропия #наука #образование
В этом анализе я буду рассматривать термодинамически замкнутые системы в том смысле, что частицы не входят в систему и не покидают её. Внутренняя энергия замкнутой системы может состоять из множества компонентов, в том числе кинетической энергии, будь то поступательные, вращательные или колебательные взаимодействия, межмолекулярные взаимодействия (часто описываемые «межмолекулярными силами» (ММС), такими как силы Лондона или водородные связи), энергии ковалентных связей или энергии решётки. Определение внутренней энергии объёмной системы — стандартная практика в классической термодинамике, помогающая нам не отслеживать, что происходит с каждой отдельной частицей или объектом, когда мы что-то делаем с замкнутой системой. Классическая термодинамика оказывается фантастическим способом анализа объёмных свойств материалов и окружающего нас мира, даже не прибегая к квантовой механике. Действительно, эти принципы были определены ещё до того, как квантовый мир начал изучаться и оцениваться в XX веке. Подводя итог поведению систем частиц в объёмных масштабах, мы введём функции состояния энтальпии, энтропии и энергии Гиббса, среди прочих, которые могут быть определены в зависимости от обстоятельств, таких как энергия Гельмгольца, как способы связи почти абстрактных понятий энергии и её распределения (или распространения) с непосредственно измеримыми величинами, которые можно определить в простых лабораторных экспериментах.
Ключевая математическая идея, рассматриваемая в этом видео, заключается в использовании концепции дифференциальной формы функции. Это способ представления бесконечно малых изменений величин через другие. Это ключевая экстраполяция школьного исчисления к рассмотрению математики изменения функций многих переменных. В термодинамике и химии эти величины включают в себя такие величины, как давление, температура и объём; Даже простое уравнение состояния идеального газа указывает на то, что эти физические величины должным образом взаимосвязаны.
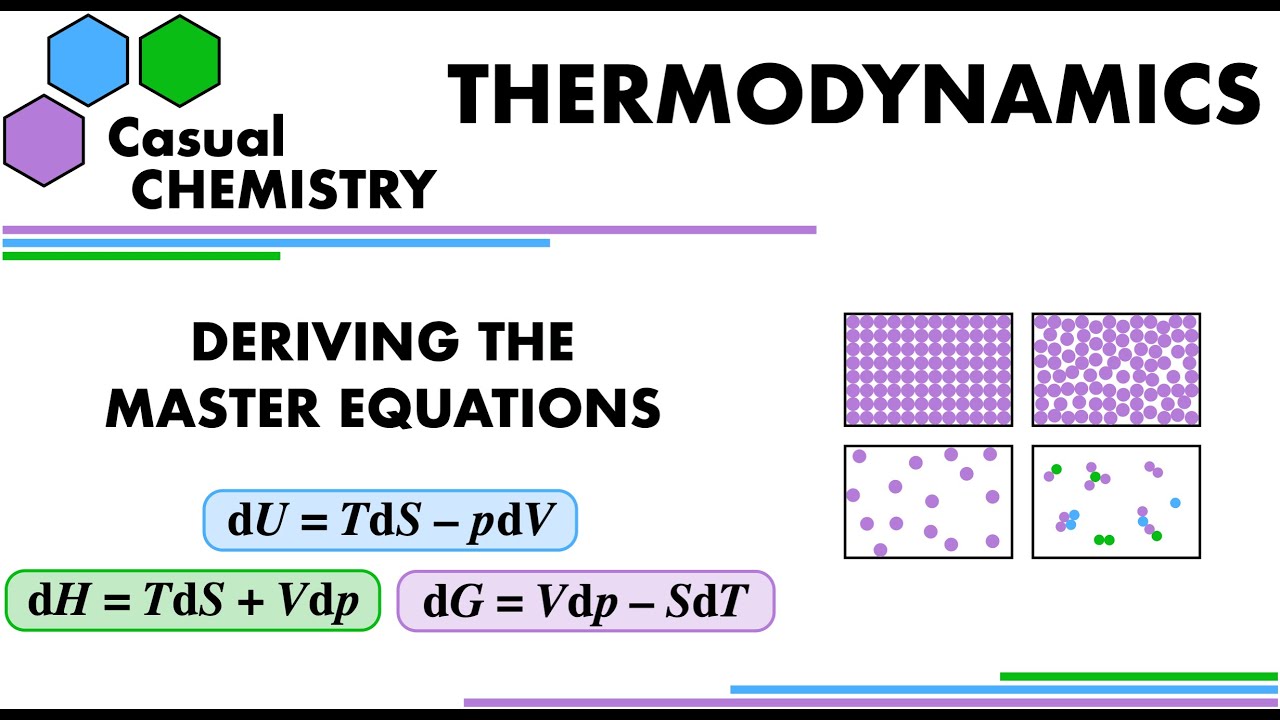
Итак, начиная с определения бесконечно малого изменения внутренней энергии как происходящего лишь от малых количеств тепла и работы, совершаемых в замкнутой системе, Основные уравнения стремятся связать этот фундаментальный принцип сохранения энергии (Первый закон термодинамики) с макроскопическими свойствами и наблюдениями. Первое Основное уравнение объединяет Первый и Второй законы термодинамики в одном выражении, напрямую связывая внутреннюю энергию как с физическими свойствами, так и с энтропией. Энтропия, по сути, является мерой распределения энергии — например, очень локализованное распределение энергии соответствует низкой энтропии.
Определение энтальпии (H) и новой функции состояния, хитроумно определяемой как H = U + pV, может связать эти объединенные Первый и Второй законы термодинамики с измеряемым изменением тепла, наблюдаемым в лабораторном эксперименте. При постоянном давлении, как это часто бывает в лабораторной химии, (обратимое) тепло, выделяющееся в ходе реакции и измеряемое термометром, отслеживающим изменение температуры, напрямую связано с изменением энтальпии. Этот анализ, в свою очередь, позволяет учёному измерить изменение энтальпии системы. Возможность определения изменений этих функций состояния путём прямых измерений во многом помогает химику предсказать, «пойдёт» ли химический процесс (будет ли он осуществимым или «самопроизвольным», если будет преодолен любой кинетический барьер). Кроме того, опытный химик может определить, как изменить экспериментальные условия, чтобы обеспечить желаемый результат запланированной реакции.
Можно вывести третье основное уравнение, которое связывает термодинамические функции состояния и физические величины другим, действительно практичным способом. Это включает введение новой функции состояния – энергии Гиббса (G), иногда называемой свободной энергией Гиббса, определяемой как G = H - TS. Бесконечно малое изменение энергии Гиббса включает в себя предыдущие результаты из второго основного уравнения, касающегося изменения энтальпии, чтобы получить дифференциальное соотношение для бесконечно малых изменений только физических величин, а именно, изменений давления и изменений объёма. Учитывая, что энергия Гиббса напрямую связана с изменением энтропии Вселенной, эта дифференциальная форма может быть использована для непосредственного применения второго закона термодинамики к экспериментальным данным.
Подобные рассуждения о математических дифференциальных формах могут быть ключевыми в научном образовании для понимания многомерного исчисления — действительно мощного инструмента как в химии, так и в физике, а также многих других способов моделирования реального мира. Эти дифференциальные формы напрямую связаны с идеями частного дифференцирования, которое всегда будет необходимо, когда функц...
Доступные форматы для скачивания:
Скачать видео mp4
-
Информация по загрузке:

















![Пожалуй, главное заблуждение об электричестве [Veritasium]](https://imager.clipsaver.ru/6Hv2GLtnf2c/max.jpg)
